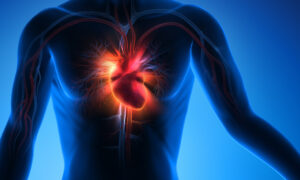
Michigan Üniversitesi tarafından yürütülen bir araştırma, pankreas kanseri hücrelerinin ölümcül büyümelerinde yakın bağ doku hücrelerini eş komplocu haline getirme şekline yeni bir ışık tutuyor.
Nature Metabolism'de ortaya çıkan bulgular, yeni terapilerle saldırıya uğrayabilecek hücreler arasındaki hayati besinlerin kanser hücrelerini aç bırakan hücreler arasındaki metabolik çapraz konuşmanın kritik bileşenlerini belirleyerek pankreas kanserine karşı yeni bir potansiyel strateji önermektedir.
Pankreas kanseri, en iyi modern tedavilere bile özellikle dirençli olmuştur; beş yıllık sağkalım oranı sadece% 10'dur.
Tümörler, sadece malign kanser hücrelerinden değil, farklı tipte hücrelerden yapılır. Birlikte çalışırlar ve sıklıkla dediğimiz gibi bir ekosistem veya mikro çevre olarak koordine olurlar. "
Deepak Nagrath, PhD., kıdemli yazar, UM'de biyomedikal mühendisliği doçenti ve UM Rogel Kanser Merkezi üyesi
Araştırma, kanser hücreleri ile yapısal, bağ dokusu hücreleri arasındaki karmaşık etkileşimleri incelemiştir; stromal hücreler olarak da bilinir -; en yaygın pankreas kanseri tümörleri içinde, pankreatik duktal adenokarsinomlar.
“Bu tümörlerde, hücrelerin yaklaşık% 90'ı aslında kanserle ilişkili fibroblastlar adı verilen bir tür stromal hücredir” diyor çalışma ilk yazarı biyomedikal mühendisliği lisansüstü öğrencisi Ziwen Zhu. "Bu hücreler, tümör etrafında lifli, koruyucu bir yapı veya hücre dışı bir matris oluşturmaya yardımcı olur ve pankreas kanserini tedavi etmeyi özellikle zorlaştıran şeylerden biridir."
Çalışma, kansere bağlı stroma hücrelerinin, besin stresi zamanlarında bu işlemi tersine çevirdiğini ve tümör mikroçevresinde bulunan hücre dışı matris proteinlerini yamyamlaştırmaya başladığını bulmuştur.
Nagrath şunları ekliyor: "Çoğu kanser tedavisi doğrudan kanser hücrelerini hedefliyor. Ancak şu ana kadar bu yaklaşım pankreas kanserinde özellikle etkili olmamıştır. Bu nedenle, standart tedavileri güçlendirmek için yeni bir strateji geliştirmeyi düşünmek heyecan vericidir; kanser hücrelerini bu diğer stromal hücrelerle etkileşimlerini hedefleyerek. "
Süreci haritalama
İnsan dolaşımdaki tümör hücresi ve doku dilimi modellerini kullanarak, araştırma ekibi kanserin kaçak büyümesi için enerji sağlayan kanser hücreleri ve kanserle ilişkili fibroblastlar arasındaki biyokimyasal değişimleri titizlikle haritaladı.
Çalışma, kanser hücrelerinin, bir enzimin üretimini uyaran fibroblastları yeniden programlayan faktörler salgıladığını gösterdi; dallı zincirli amino asit aminotransferaz (BCAT1) -; bu, fibroblastların mevcut dallı zincirli amino asitleri (BCAA) kanser hücrelerinin, dallı zincirli alfa-ketoasitlerin (BCKA'lar) tercih edilen yakıta dönüştürmesine izin verir.
Nagrath, "Şaşırtıcı bir şekilde bulduğumuz şey, BCAT1'in ağırlıklı olarak kanser hücrelerinde değil stromal hücrelerde eksprese edilmesidir." Diyor. "Kanser hücreleri bu dallı zincirli amino asitleri, BCAA'ları çok verimli bir şekilde kullanamazlar. Bunun yerine, stromal hücrelerin BCAA'ları metabolize edebilen ve parçalayabilen ve dönüştüren enzimi daha fazla üretmelerine neden oluyorlar. tümör mikro ortamında mevcut hücre dışı matris proteinleri kullanarak ketoasitlere – BCKA'lara – stromal hücreler daha sonra bu kanser hücrelerinin, sürekli büyümeleri için protein ve enerji ihtiyaçlarını karşılamak üzere metabolize edebilecekleri BCKA'ları salgılarlar. "
Yeni ilaç hedefleri
Araştırma ekibi, pankreas kanseri hücrelerini doğrudan zehirlemek ve öldürmek için bir ilaç aramak yerine, bu besin döngüsünü bozmak ve kanser hücrelerini açlıktan ölmek için seçenekler araştırdı.
Takım bulundu ilaç gabapentin -; fibroblastlardaki kritik enzim BCAT1'i inhibe eden sentetik bir amino asit; kanser hücrelerinin ihtiyaç duyduğu ketoasitlerin üretimini azalttı.
"Gabapentin, sinir ağrısını tedavi etmek için yaygın ve iyi bilinen bir ilaçtır, bu nedenle bu yeni bilgiyi klinikte kullanım için potansiyel olarak tercüme etmenin yolu, yeni, kanıtlanmamış bir bileşikle başlıyor olmamızdan çok daha kısadır" diyor Nagrath.
Araştırmacılar ayrıca kanser hücrelerinde aktif olan potansiyel bir ortak hedef belirlediler, ancak mevcut ilaçların onu hedeflediği bilinmemektedir.
"Bu nedenle, gelecekteki çalışmanın bir başka yönü, dallı zincirli alfa-ketoasit dehidrojenaz kompleksi (BCKDHC) olarak bilinen kanser hücrelerinde bir protein kompleksini bozmak için küçük moleküllü bileşikler geliştirmeye çalışmak olacaktır." "Neyse ki, UM harika bir ilaç keşif programı var."
Deneyler iki farklı hastadan türetilmiş hücre modeli kullanılarak gerçekleştirilmiştir; pankreas kanseri olan hastalardan dolaşımdaki tümör hücresi organoidleri ve doku dilimleri.
Modeller -; ortak yazarlar Sunitha Nagrath, UM'de kimya mühendisliği profesörü ve Ted Lawrence, MD, Ph.D., Isadore Lampe Profesörü ve Michigan Medicine'de radyasyon onkolojisi başkanı ile işbirliği içinde geliştirildi; Deepak Nagrath, hasta tümörlerine güçlü benzerlikleri nedeniyle seçildi ve ekibin araştırma sorularını cevaplamaya çok uygun olduğunu belirtti.
Zhu, Z., vd. (2020) Tümörle yeniden programlanan stromal BCAT1, stromalce zengin PDAC tümörlerinde dallı zincirli ketoasit bağımlılığını arttırır. Doğa Metabolizması . doi.org/10.1038/s42255-020-0226-5 .

You must be logged in to post a comment Login
Leave a Reply
Yorum yapabilmek için oturum açmalısınız.